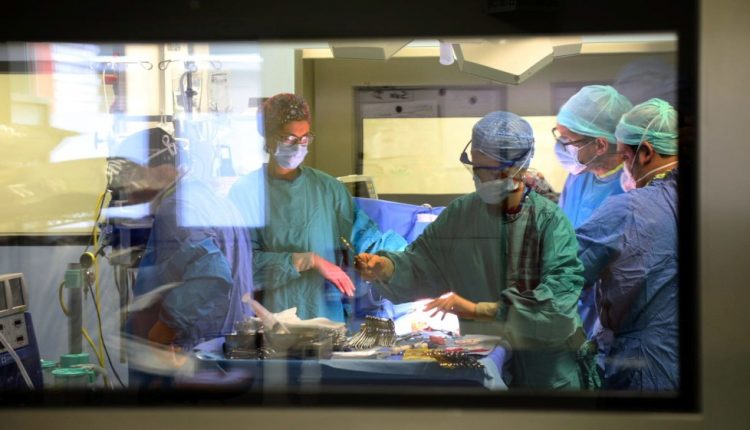
Transplante de órgãos: em que consiste, quais são as etapas e o que o futuro reserva
O transplante de órgãos é o procedimento cirúrgico pelo qual um ou mais órgãos doentes (cuja funcionalidade não é mais recuperável) são substituídos por um ou mais órgãos retirados de um doador (cadavérico ou vivo)
Uma operação que tem as suas raízes, conceptualmente, nos primórdios da história da humanidade (foi falada pela primeira vez pelos médicos chineses), é, no entanto, uma solução terapêutica muito recente: o conhecimento que a tornou possível (imunologia, estudo de antigénios…) adquirido apenas no início do século XX.
A partir de 1950, o transplante tornou-se uma opção consagrada no tratamento daquelas patologias que levam à destruição irreparável do órgão e, portanto, à morte do paciente.
Mas o transplante não é apenas a última perspectiva para aqueles cujas vidas estão em perigo: esta operação também permite melhorar a qualidade de vida dos pacientes que sofrem de doenças crônicas incapacitantes (por exemplo, transplante renal para pacientes dialisados).
O futuro dos transplantes ainda está para ser esboçado, mas está muito claro na mente de cientistas e médicos envolvidos na pesquisa: implantação de órgãos artificiais ou de órgãos retirados de animais geneticamente modificados (xenotransplante), clonagem e implantação de células-tronco são apenas alguns exemplos das direções em que a paisagem científica do mundo está se movendo.
Cirurgia de transplante de órgãos
A palavra 'transplante' muitas vezes indica, de forma redutiva, a operação de substituição de um órgão doente por um saudável.
Na realidade, há toda uma organização e preparação por trás desta operação que envolve extrema precisão e sincronização de pessoas e instrumentos.
A prática da operação difere dependendo do doador: se a retirada do órgão for de uma pessoa viva, de fato, é possível planejar a operação; o que obviamente não é viável se os órgãos provêm de um doador cadavérico, que morreu de causas acidentais e imprevisíveis.
Assim que a comissão médica obtiver o consentimento da família e declarar a ocorrência da morte encefálica do potencial doador, inicia-se a avaliação de seus dados: compatibilidade com potenciais receptores nas listas de espera, histórico médico, características imunológicas, grupo sanguíneo, etc.
O transplante de órgãos se desenvolve através de várias etapas
FASE 1
Uma pessoa com lesões que podem ser doadoras (por exemplo, uma lesão na cabeça muito grave) é internada em terapia intensiva.
Um médico fala com a família sobre a possibilidade de doar seus órgãos; caso estejam disponíveis, é imediatamente avisado o centro de coordenação, que se encarrega de informar o potencial doador e identificar o potencial receptor.
Enquanto isso, são avaliados os dados do paciente doador: compatibilidade com potenciais receptores da lista, histórico médico, características imunológicas. Inicia-se o período de observação de 6 horas, obrigatório antes da certificação de morte encefálica.
FASE 2
A equipe de explantação é acionada e deve estar disponível em pouco tempo.
Os médicos geralmente chegam às instalações de helicóptero. Enquanto isso, no hospital onde será realizado o transplante, o receptor é chamado para realizar diversos exames e avaliar seu estado de saúde.
Inúmeras verificações também são realizadas nos órgãos a serem doados para evitar a transmissão de doenças infecciosas ou tumores do doador para o receptor.
FASE 3
Ao final do período de observação, se todos os indícios apontarem para o diagnóstico de morte encefálica irreversível, pode-se iniciar o explante (aproximadamente 2 horas).
O receptor entra na sala de cirurgia e está preparado para a operação. A administração de drogas imunossupressoras começa agora para evitar que os linfócitos reconheçam o órgão como estranho e causem rejeição.
FASE 4
O órgão finalmente chega, imerso em uma solução especial para proteger suas células e transportado em um recipiente especial cheio de gelo para desacelerar sua atividade celular.
Uma equipe de médicos prepara o receptor, a outra cuida da limpeza do órgão a ser transplantado.
FASE 5
O transplante já pode começar: os vasos sanguíneos estão conectados, o sangramento é controlado.
PASSO 6
O paciente sai da sala de cirurgia, mas ainda está sob anestesia, que será prolongada por pelo menos mais 6 a 8 horas para permitir que o novo órgão se acostume com a diferença de temperatura entre o recipiente com o gelo e o corpo e, é claro, para o próprio órgão.
O paciente permanece conectado à máquina para respirar.
PASSO 7
O paciente acorda na unidade de terapia intensiva; se seu estado geral for bom, ele é retirado do respirador artificial.
Após cerca de 4 dias, ele começa a andar novamente e a comer.
Após cerca de 10 dias, ele poderá deixar o hospital e viver com seu novo órgão.
Inicialmente, ele terá que retornar ao hospital todos os dias para exames imunológicos; depois de um ano, ele poderá retornar uma vez a cada dois meses.
Remoção de órgãos
Uma vez constatada a morte encefálica e obtido o consentimento da família (no caso de falta de vontade expressa do doador), o potencial doador deixa de ser assistido pelo respirador mecânico e os órgãos podem ser colhidos para transplante no mesmo hospital que estabeleceu a idoneidade .
A equipe previamente alertada entra no bloco operatório para a operação de remoção.
Opor-se à remoção nunca significa ajudar o paciente a ter um melhor atendimento; o cuidado, de fato, termina no momento em que a morte encefálica é estabelecida; opor-se a ela significaria, portanto, apenas privar outra pessoa de uma vida melhor graças a um novo órgão.
Hoje, outro tipo de transplante também está ganhando espaço, o de pessoas vivas.
De fato, agora é possível levar um rim, fígado ou lobo pulmonar para transplante em pessoas particularmente em risco que não sobreviveriam na lista de espera.
Geralmente são crianças, tanto pela escassez de órgãos pediátricos para transplante quanto pelo pequeno tamanho, o que também significa que o doador não corre um risco muito alto.
Uma vez retirados, os órgãos requerem procedimentos especiais para preservá-los para transplante.
Há, para cada órgão, um tempo máximo de preservação, além do qual os tecidos, não mais recebendo sangue e, portanto, oxigênio, entram em necrose, ou seja, suas células morrem e, portanto, ficam inutilizáveis.
Esses tempos variam de órgão para órgão: coração (4-6 horas), pulmão (4-6 horas), fígado (12-18 horas), rim 48-72 horas, pâncreas (12-24 horas).
Transplante de órgãos: rejeição
A rejeição é a reação que o organismo receptor tem em relação ao órgão ou tecido transplantado.
Na verdade, o sistema imunológico do receptor reconhece o órgão como estranho e o ataca como se fosse um patógeno.
Existem quatro tipos de rejeição
- rejeição hiperaguda: é a mais rápida e ocorre em poucos minutos ou horas após o transplante;
- rejeição acelerada: ocorre frequentemente em pacientes que já receberam um transplante anterior e ocorre 3-4 dias após a operação;
- rejeição aguda: ocorre após um período de tempo que varia de 5 a 90 dias; sintomas específicos são edema, febre e perda de função do órgão transplantado;
- rejeição crônica: desenvolve-se cerca de 3 meses após o transplante e pode causar dano tecidual ao novo órgão a ponto de perda de função.
Experimentar a rejeição do órgão transplantado não significa necessariamente perdê-lo inevitavelmente; pelo contrário, a rejeição é tratada com sucesso se forem tomadas medidas dentro de um prazo razoável por meio do uso de drogas imunossupressoras.
Os imunossupressores que o médico prescreve após o transplante ajudarão o órgão transplantado a não correr o risco de rejeição e a permanecer saudável.
Como as células do sistema imunológico são diferentes, os medicamentos prescritos para imunossupressão também serão diferentes.
Indicações e contra-indicações para transplante de órgãos
A maior e mais imediata indicação para transplante é a falência irreversível de órgãos vitais como rins, fígado, pulmões, pâncreas, mas também córneas, medula óssea, intestinos.
De fato, nesses casos, o transplante é o único tratamento eficaz para garantir a sobrevida.
Portanto, qualquer condição patológica que impeça o funcionamento do órgão de modo a ameaçar a sobrevida do paciente deve ser considerada uma indicação para transplante.
Cuidados pós-operatórios
Após o transplante, os receptores são admitidos nos primeiros dias em uma enfermaria equipada para terapia intensiva, onde é iniciada a terapia imunossupressora.
O paciente imunossuprimido necessita de isolamento em salas 'estéreis', especialmente criadas para evitar qualquer tipo de contaminação do ambiente externo.
A 'caixa' na qual o receptor é admitido após a operação de transplante fica completamente isolada do restante da unidade de reanimação utilizada para cirurgia convencional.
A condição de isolamento estrito persiste pelo tempo necessário para que o paciente supere a fase crítica pós-cirúrgica (geralmente 5-6 dias), ou nos casos em que seja necessária terapia anti-rejeição.
Visitas a pacientes transplantados
No pós-operatório imediato, são permitidas visitas a familiares próximos, desde que devidamente trajados (conforme procedimentos de entrada em sala limpa).
Cada pessoa é admitida na zona de filtro uma de cada vez e, claro, pessoas com suspeita e/ou evidência de doenças infecciosas não podem ser admitidas.
Desenvolvimentos futuros
As questões mais graves na medicina de transplantes são, por um lado, a rejeição do órgão transplantado e, por outro, a insuficiência dos órgãos doados em relação aos necessários.
Em ambas as direções, a pesquisa está experimentando várias soluções para superar esses problemas.
No que diz respeito à rejeição, procura-se criar soluções que consigam enganar o sistema imunitário, reduzindo assim a terapêutica imunossupressora actualmente em uso, ou que protejam o órgão transplantado do ataque dos linfócitos T, responsáveis pela eliminação de agentes fora do organismo .
Por outro lado, a escassez de órgãos, órgãos artificiais, engenharia de tecidos ou xenotransplantes estão sendo experimentados que podem substituir órgãos humanos.
Terapia de genes
Por meio da terapia gênica, é possível ir até a origem do problema e eliminar os defeitos genéticos diretamente nas células, tecidos ou órgãos afetados.
O gene saudável é introduzido diretamente no local afetado, onde começa a produzir aquelas substâncias que o corpo doente não consegue produzir por conta própria.
No entanto, a terapia gênica ainda está longe de ser utilizada. Para poder transportar DNA estranho para o núcleo da célula, são necessários 'vetores' especiais - vírus que perderam suas características infecciosas, mas ainda são capazes de atacar as células e transmitir-lhes sua herança genética.
Para evitar a rejeição, o órgão a ser transplantado teria que ser tratado em laboratório, transferindo para ele genes que o tornariam capaz de se defender do sistema imunológico do receptor.
Agora os genes são conhecidos, mas ainda não são manuseados com a precisão necessária. O próximo passo será buscar a combinação perfeita de genes que impeça a ação de todos os mecanismos imunológicos do receptor.
Engenharia de tecidos
O objetivo deste tipo de terapia é encontrar uma alternativa aos órgãos humanos.
Já agora, os pesquisadores são capazes de produzir tecidos como vasos sanguíneos, válvulas cardíacas, cartilagem e pele em laboratório.
Foi possível superar essa nova fronteira graças ao fato de que as células tendem a se agregar para formar órgãos e tecidos.
Células-tronco
As células-tronco são as células indiferenciadas encontradas em embriões humanos uma semana após a fertilização.
São também as células 'iniciais' a partir das quais se desenvolverão os tecidos e órgãos da criança que vai nascer.
Sua função é regular a renovação das células sanguíneas (glóbulos vermelhos, glóbulos brancos e plaquetas) e as do sistema imunológico (linfócitos).
Hoje, máquinas computadorizadas, separadoras, são usadas para coletar essas células, permitindo a seleção das células necessárias. Os receptores das células são pacientes que sofrem de doenças de pele, doenças do sangue ou tumores sólidos.
Além do fato de as células-tronco ainda serem amplamente desconhecidas, há também um problema ético: a colheita de células-tronco embrionárias implica a morte do embrião.
É por isso que a maneira de colher células-tronco de adultos está sendo aperfeiçoada.
Clonagem
A técnica de clonagem permitiria contornar completamente o problema da rejeição de órgãos.
Envolveria a introdução do núcleo da célula do paciente, com toda a sua herança genética, na célula-tronco de um embrião ou oócito humano que antes não tinha núcleo próprio.
Cultivadas in vitro em laboratório, essas células modificadas seriam geneticamente idênticas às do sistema imunológico do paciente, que não as reconheceria como estranhas.
Esta técnica não é uma opção viável no momento porque tanto a clonagem, a colheita de células-tronco e o uso indiscriminado de oócitos são proibidos por lei.
Xenotransplante
O xenotransplante, ou seja, o transplante de células, tecidos e órgãos animais para humanos, parece ser a solução futura para a escassez de órgãos para transplante.
As experiências neste campo são numerosas e enfrentam problemas éticos, psicológicos e, por último, mas não menos importantes, imunológicos.
As poucas tentativas que foram feitas, de fato (um fígado de porco e um coração de babuíno transplantados em dois seres humanos diferentes) não deram os resultados desejados.
A crise de rejeição, de fato, foi particularmente violenta e impossível de controlar.
No entanto, esta técnica pode realmente ser a solução para a escassez de órgãos.
Na verdade, o que mais se teme é o desenvolvimento de infecções tipicamente animais, transferidas para humanos por meio de patógenos presentes no órgão a ser transplantado, o que pode ser desastroso.
Uma possível alternativa a esta desvantagem poderia ser modificações genéticas em animais doadores; na prática, os animais seriam criados em ambiente estéril e geneticamente modificados para tornar seus órgãos mais compatíveis com o organismo do receptor.
Por enquanto, no entanto, alguns marcos foram alcançados; trata-se de xenotransplantes de células e não de xenotransplantes de órgãos, como células embrionárias de porco para o tratamento da doença de Parkinson, células de medula de babuíno transplantadas em pacientes terminais de AIDS na tentativa de recuperar o sistema imunológico dos pacientes, ou ínsulas de pâncreas ainda de porcos na estimulação da produção de insulina como terapia contra o diabetes.
Transplante de órgãos: órgãos artificiais
Outra solução para a falência de órgãos, como a rejeição, são os órgãos artificiais.
O principal problema é a compatibilidade biológica; estes são, afinal, órgãos mecânicos que precisam se adaptar a um organismo biológico.
A biocompatibilidade deve abranger todas as características morfológicas, físicas, químicas e funcionais que sejam capazes de proporcionar a funcionalidade do órgão e, ao mesmo tempo, sua sobrevivência sem risco de rejeição.
São todas essas implicações que tornam complexa a produção de órgãos artificiais capazes de substituir completa e perfeitamente os órgãos 'naturais' em suas funções.
Leia também:
Emergency Live Even More ... Live: Baixe o novo aplicativo gratuito do seu jornal para iOS e Android
Transplante de Órgãos: Diagnóstico e Cuidados de Pacientes em Espera
O que é transplante cardíaco? Uma visão geral
Como é feito um transplante de rosto? - VÍDEO



