Dışkı bakteriyoterapisi: Clostridium difficile, kolit ve Crohn hastalığı için dışkı nakli
Dışkı nakli veya dışkı transfüzyonu veya insan probiyotiklerinin (HPI) infüzyonu veya dışkı mikrobiyom nakli olarak da bilinen dışkı bakteriyoterapisi, psödomembranöz kolitten muzdarip deneklerde bir miktar etkinlikle kullanılan deneysel bir aşamada farmakolojik olmayan bir tıbbi tedavidir. Clostridium difficile bakterisi (yakın zamanda 'Clostridium difficile' olarak yeniden adlandırıldı); veya yaygın tedavilere dirençli ülseratif kolit vakalarında bile
Bu yenilikçi tedavinin amacı, sağlıklı bir donörün dışkısından veya bazı durumlarda aynı kişi tarafından daha önce 'bağışlanan' dışkıdan alınan sağlıklı (dengeli) bir insan mikrobiyotasını yeniden ortaya koyarak kolonun mikrobiyal ekolojisini ve homeostazını eski haline getirmektir. gastrointestinal floranın homotransfüzyonu veya otolog restorasyonu - ARGF).
Bu terapötik tekniğin teorik mantığı, probiyotiklerin kullanımına ilişkin en gelişmiş araştırmalarda ve belirli bir ortamda (bu ortamda bulunan) bakteriler, arkebakteriler, mantarlar, virüsler gibi mikroorganizmalar kümesi olan mikrobiyom üzerine yapılan çalışmalarda bulunabilir. dışkı ortamı durumunda).
İyi bir mikrobiyal ekolojinin patojenik organizmaların aşırı büyümesini nasıl engelleyebileceği iyi bilinmektedir.
Kolonda, toplam 500 bakteri ile 1000 ila yaklaşık 1013 farklı bakteri türü olduğu tahmin edilmektedir.
Aslında, mikrobiyom, konakçı organizma ile simbiyoz olan kendi başına biyolojik bir varlık olarak düşünülmelidir.
Bakteri kompleksi veya mikrobiyom, konakçı organizmanın homeostazını korumada görev yapar; bu mikrobiyal flora vücuda yeniden verildiğinde nispeten zararsızdır.
Mikrobiyomun rolü hakkında pek bir şey bilinmemekle birlikte, birçok otçul ve otçul olmayan hayvan türünün, muhtemelen çift sindirim döngüsüne (çift sindirim) sahip olmaları nedeniyle koprofajik alışkanlıkları olduğu bilinmektedir.
Dışkı nakli: Dışkı bakteriyoterapisinin ana avantajı, yüksek oranda patojenik bakterilerde antibiyotik direncine neden olma riskini azaltmaktır.
Diğer avantajlar, antibiyotik direncinin mevcut olduğu vakaların tedavisi için nispeten düşük maliyet, ilaca ihtiyaç olmaması ve iyi etkinliktir (ancak daha büyük çalışmalarla teyit edilecektir).
Bununla birlikte, yöntem, geleneksel antibiyotik tedavisine kıyasla daha fazla invaziv olması ve potansiyel enfeksiyon bulaşma riskleri (bakteriler, virüsler, prionlar, bağırsak parazitleri) nedeniyle hala 'son çare' tedavisi olarak kabul edilmektedir.
Fekal bakteriyoterapi ile ilgili deneyim hala sınırlı olsa da, prosedürle ilgili yayınlanan sonuçlar, 80'den fazla hastanın ortalama %90'ın üzerinde bir başarı oranı gösterdiğini göstermektedir.
Fekal bakteriyoterapi, tekrarlanan antibiyotik kullanım döngülerini kırabilen, düşük teknolojili, gerçekleştirmesi kolay bir prosedürdür ve bu da son zamanlarda artan antibiyotik direnci oluşma riskini azaltır.
Aynı zamanda, gerekli hastaneye yatışlarla birlikte tekrarlanan antibiyotik uygulamalarına kıyasla maliyet tasarrufu sağlama potansiyeline de sahiptir.
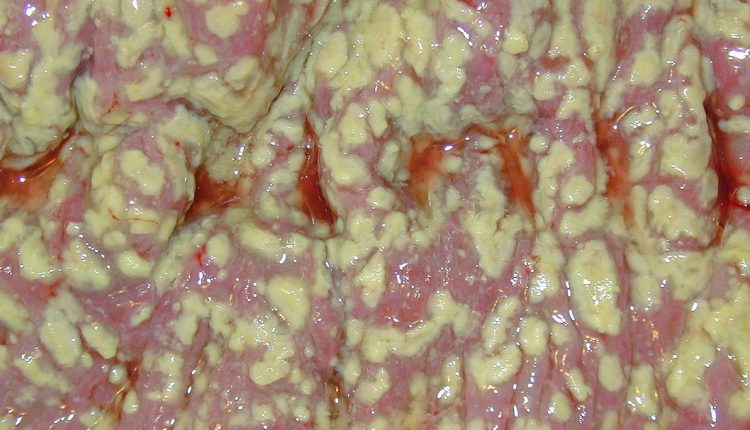
Psödomembranöz kolit
Clostridium difficile'nin (CDI) bir patojeni olarak önemi 1978'den beri kesin olarak kanıtlanmıştır, ancak bu tekniğin psödomembranöz kolit tedavisindeki önemi aynı zamanda epidemiyolojisinin son zamanlarda değişmesinden ve klinisyenler için ciddi teşhis ve tedavi sorunları oluşturmasından kaynaklanmaktadır. .
Enfeksiyon oranları (CDI) 31'da 100,000/1996'den 61'te 100,000/2003'e iki katına çıktı.
Son yıllarda, C. difficile CDI enfeksiyonunun şiddeti ve ölüm oranı artmaktadır ve bu, Kuzey Amerika Pulsed-field jel elektroforez tip 1 (NAP-1) suşu olarak bilinen yeni bir öldürücü C. difficile suşuna atfedilmiştir. ayrıca PFGE tipi BI/NAP1 ribotipi 027.
NAP-1 suşunun benzersizliği, A ve B toksinlerinin artan üretiminde ve ikili toksin üretiminde ve florokinolon direncinde yatmaktadır.
C. difficile'nin hipervirülent NAP1 suşları, son zamanlardaki nozokomiyal salgınların çoğundan sorumludur ve florokinolon antibiyotiklerin yaygın kullanımı, bu suşun seçici çoğalmasını kolaylaştırmış olabilir.
NAP1 suşunun ayrıca belirgin lökositoz, akut böbrek yetmezliği, hemodinamik instabilite ve toksik megakolon ile karakterize şiddetli, fulminan kolite neden olma olasılığı daha yüksektir.
C. difficile nozokomiyal diyarenin en yaygın bakteriyel nedeni haline gelmiştir.
Clostridium difficile enfeksiyonu, özellikle antibiyotik tedavisi gören hastalarda veya kök hücre nakli yapılan kanser hastalarında ve hatta radyoterapi gören hastalarda önemli morbidite ve mortaliteye neden olan ciddi bir tıbbi durum olan CDAD'ye (Clostridium difficile Associated Disease) veya daha nadiren psödomembranöz kolite neden olur. .
Hipervirülan C. difficile suşlarının neden olduğu enfeksiyon sıklığının artması, metronidazol ve vankomisin ile geleneksel tedavide komplikasyonlara ve terapötik başarısızlıklara yol açmıştır.
Sınırlı klinik deneyime rağmen, fekal bakteriyoterapinin yüksek klinik iyileşme oranları sağladığı ön olarak gösterilmiş olsa da, bugüne kadar bu terapötik yaklaşım için randomize klinik çalışmalar eksiktir.
Ülseratif kolit
Ülseratif kolitte bugüne kadar hiçbir patojen bulunamamıştır.
Ancak bu durumda fekal bakteriyoterapinin etkinliği, ülseratif kolitin nedeninin bilinmeyen kalan bir patojenle önceki bir enfeksiyondan kaynaklanabileceğini düşündürür.
Gerçekten de, bu hastalarda ilk enfeksiyon muhtemelen doğal olarak düzelmiş olabilir; ancak bazen, kalın bağırsağın bağırsak florasındaki bir dengesizlik, iltihabik bir alevlenmeye neden olabilir (bu, bu hastalığın döngüsel ve tekrarlayan doğasını açıklayabilir).
Bu döngü, en azından birçok durumda, sağlıklı bir bağırsaktan (heterograft) alınan bir bakteri kompleksi (probiyotik) ile hastanın kolonunun yeniden kolonize edilmesiyle kesintiye uğruyor gibi görünmektedir.
Bazı doktorlar, sağlıklı deneklerde uygulanan bu tedavinin güvenli olduğuna ve birçok hastanın bu yenilikçi tedaviden fayda görebileceğine inanmaktadır.
Mayıs 2011'de yapılan bir araştırma, ülseratif kolitli çocukların ve ebeveynlerinin, yönteme yönelik ilk hoşnutsuzluklarının üstesinden geldikten sonra bu tedaviyi kabul etmeye istekli olduklarını doğruladı.
2013 yılında başka bir araştırma, 7-21 yaşları arasındaki on denekte ileriye dönük bir pilot çalışma ile tedavinin geçerliliğini doğruladı.
Bu çalışma, ülseratif kolitte dışkı nakli tedavisinin tolere edilebilirliğini ve etkinliğini göstermektedir; aslında yedi denekte bir hafta içinde klinik remisyon oldu ve dokuz kişiden altısı bir ayda klinik remisyonu sürdürdü.
Dışkı nakli, dışkı bakteriyoterapisi için çalışılan diğer hastalıklar
Teknik şu anda Parkinson hastalığı, diyabet, obezite, irritabl bağırsak sendromu, kronik inflamatuar bağırsak hastalığı, multipl skleroz, idiyopatik trombositopenik purpura, Crohn hastalığı, insülin direnci ve kronik yorgunluk sendromu olan kişilerde incelenmektedir.
Klasik prosedür
Normalde hastanın yakın, sağlıklı bir akrabasının dışkısı, bulaşıcı bakteri veya virüslerin veya Salmonella, hepatit virüsü, vb. gibi parazitlerin varlığı araştırıldıktan ve dışlandıktan sonra kullanılır.
Dışkı örneği alındıktan sonra klinik bir laboratuvarda işlenir ve sıvı bir süspansiyon şeklinde hazırlanır ve daha sonra çekum seviyesine kadar çıkan bir nazogastrik tüp aracılığıyla üst gastrointestinal sisteme damlatılır.
Prosedür bazen sağlıklı bir donörün dışkısından insan mikrobiyotası ile yapılan lavmanlarla 5-10 günlük tedaviyi içerir; çoğu hasta sadece bir tedaviden sonra iyileşir.
En iyi donör seçimi, çok çeşitli bakteriyel ve parazitik ajanlar için test edilmiş yakın bir akrabadır.
Lavmanlar, gerekli tüm bakımı sağlamak için hastane ortamında hazırlanır ve uygulanır.
Probiyotiğin infüzyonu, bakterileri doğrudan ince bağırsağa ileten bir nazogastrik tüp yoluyla da yapılabilir.
En iyi sonucu elde etmek için iki yöntem birleştirilebilir.
İşlemden bir yıl sonrasına kadar düzenli kontroller yapılmalıdır.
ARGF (gastrointestinal floranın otolog restorasyonu)
Gastrointestinal floranın (ARGF) otolog restorasyonu, şu anda geliştirilmekte olan değiştirilmiş bir fekal bakteriyoterapi şeklidir.
Bu yöntem daha güvenli, daha etkili ve uygulaması daha kolaydır.
Tıbbi tedaviden önce hasta tarafından otolog (kendi) dışkı örneği verilir ve buzdolabında saklanır.
Hastada daha sonra C. difficile patolojisi gelişirse, numune salinle ekstrakte edilir ve filtrelenir. Süzüntü liyofilize edilir ve nihai katı gastro-dirençli kapsüller içine alınır.
Kapsüllerin uygulanması, oluşmuş olabilecek herhangi bir C. difficile enfeksiyonuyla mücadelede yararlı olan, hastanın kendi kolon florasını eski haline getirir.
Bu prosedür, donör tarafından hastaya olası bir enfeksiyonun bulaşabileceği klasik fekal bakteriyoterapi risklerini ortadan kaldırır ve ayrıca fekal numunenin bir gastrik prob aracılığıyla duodenuma verilmesi ihtiyacını da ortadan kaldırır.
etki
Yöntemin psödomembranöz kolit nükslerini önlemedeki etkinliğinin %90 civarında olduğu tahmin edilmektedir.
Aralık 2011'de yapılan bir çalışma, tekrarlayan C. difficile enfeksiyonları olan 92 hastadan oluşan bir grupta ishali veya daha fazla nüksü önlemede yöntemin %26'lik bir etkinliğini gösteren bu verileri doğrulamaktadır.
2011'de Finlandiya'da yapılan bir araştırma, tekrarlayan Clostridium difficile enfeksiyonlarının (CDI) antibiyotik tedavisinin hastaların %50'sinde nükslere yol açtığına işaret ediyor.
Polietilen glikol (lavaj) ile bağırsak hazırlığından sonra bir kolonoskopi test prosedürü sırasında dışkı naklinin kullanılması, bir yıllık takipte tekrarlayan psödomembranöz kolit vakalarının %89'unun çözülmesiyle sonuçlanmıştır ve tedavi edilen vakaların bir neden olduğunu vurgulamaktadır. özellikle öldürücü C. difficile suşu (tip 027).
Yine Aralık 2011'de, 317 hasta üzerinde yapılan bir inceleme, yöntemin %92 etkili olduğunu ve ayrıca çok az yan etki gösterdiğini gösterdi.
2015 yılında, vankomisin ile bakteriyel dışkı tedavisinin bu antibiyotiğe üstünlüğünü gösteren bir karşılaştırma çalışması yayınlandı.
Ayrıca Oku
Kolit: Belirtileri, Tedavisi ve Ne Yenir?
Ülseratif Kolit: Nedenleri, Belirtileri ve Tedavisi
Bir Bebeğin Bağırsak Bakterileri Gelecekteki Obeziteyi Tahmin Edebilir
Dışkı Mikrobiyota Nakli (Dışkı Nakli): Ne İçin Yapılır ve Nasıl Yapılır?
Bologna'da (İtalya) Sant'Orsola, Mikrobiyota Nakli ile Yeni Bir Tıbbi Sınır Açıyor
Beyni Bağırsak İltihabından Koruyan 'Kapı'nın Rolü, Mikrobiyota Keşfedildi
Divertikülit ve Divertiküloz Arasındaki Farklar Nelerdir?
Kolonoskopi: Son Teknikler ve Çeşitli Tipler
Disbiyoz ve Hidrokolon Tedavisi: Bağırsak Sağlığı Nasıl Geri Getirilir
Kapsül Endoskopi: Nedir ve Nasıl Yapılır?
Kolonoskopi Nedir, Ne Zaman Yapılır, Hazırlanması ve Riskleri
Kolon Yıkama: Nedir, Ne İçindir ve Ne Zaman Yapılması Gerekir?
Rektosigmoidoskopi ve Kolonoskopi: Nedirler ve Ne Zaman Yapılırlar?
Ülseratif Kolit: Bağırsak Hastalığının Tipik Belirtileri Nelerdir?
Galler'de Bağırsak Cerrahisi Ölüm Oranı 'Beklenenden Yüksek'
İrritabl Bağırsak Sendromu (IBS): Kontrol Altında Tutulması Gereken Benign Bir Durum
Bağırsak Enfeksiyonları: Dientamoeba Fragilis Enfeksiyonu Nasıl Bulaşır?
Çalışma Kolon Kanseri ve Antibiyotik Kullanımı Arasındaki Bağlantıyı Buldu
Kolonoskopi: Yapay Zeka ile Daha Etkili ve Sürdürülebilir
Kolorektal Rezeksiyon: Hangi Durumlarda Kolon Yolunun Çıkarılması Gereklidir
Gastroskopi: Muayene Ne İçin Yapılır ve Nasıl Yapılır?
Gastro-Özofagus Reflü: Belirtileri, Teşhis Ve Tedavi
Endoskopik Polipektomi: Nedir, Ne Zaman Yapılır?
Düz Bacak Kaldırma: Gastroözofageal Reflü Hastalığını Teşhis Etmek İçin Yeni Manevra
Gastroenteroloji: Gastro-Özofageal Reflü İçin Endoskopik Tedavi
Özofajit: Belirtileri, Tanı ve Tedavisi
Gastroözofageal Reflü: Nedenleri ve Çözümleri
Gastroskopi: Nedir ve Ne İçindir?
Kolonik Divertiküler Hastalık: Kolonik Divertiküloz Tanı ve Tedavisi
Gastro-Özofageal Reflü Hastalığı (GÖRH): Belirtileri, Tanı ve Tedavisi
Divertikül: Divertikülit Belirtileri Nelerdir ve Nasıl Tedavi Edilir?
İrritabl Bağırsak Sendromu (IBS): Kontrol Altında Tutulması Gereken Benign Bir Durum
Gastroözofageal Reflü: Nedenleri, Belirtileri, Tanı ve Tedaviye Yönelik Testler
Hodgkin Dışı Lenfoma: Heterojen Bir Tümör Grubunun Belirtileri, Tanısı ve Tedavisi
Helicobacter Pylori: Nasıl Tanınır ve Tedavi Edilir



